Електрически ток в течности и газове
Електрически ток в течности
 В метален проводник електричество се образува от насоченото движение на свободните електрони и че не настъпват промени в веществото, от което е направен проводникът.
В метален проводник електричество се образува от насоченото движение на свободните електрони и че не настъпват промени в веществото, от което е направен проводникът.
Такива проводници, при които преминаването на електрически ток не е придружено от химически промени в тяхното вещество, се наричат първокласни водачи… Те включват всички метали, въглища и редица други вещества.
Но в природата има и такива проводници на електрически ток, при които възникват химически явления по време на преминаването на тока. Тези проводници се наричат водачи от втори вид… Те включват главно различни разтвори във вода на киселини, соли и основи.
Ако излеете вода в стъклен съд и добавите няколко капки сярна киселина (или някаква друга киселина или алкал) към нея, а след това вземете две метални пластини и прикрепете проводници към тях, като спуснете тези плочи в съда, и свържете ток източник към другите краища на проводниците през превключвателя и амперметъра, тогава газът ще се освободи от разтвора и той ще продължи непрекъснато, докато веригата е затворена. подкислената вода наистина е проводник. Освен това плочите ще започнат да се покриват с газови мехурчета. Тогава тези мехурчета ще се отделят от плочите и ще излязат.
Когато електрически ток преминава през разтвора, настъпват химически промени, в резултат на което се отделя газ.
Наричат се проводници от втори вид електролити, и явлението, което се случва в електролита, когато през него преминава електрически ток, е електролиза.
Металните плочи, потопени в електролит, се наричат електроди; един от тях, свързан с положителния полюс на източника на ток, се нарича анод, а другият, свързан с отрицателния полюс, е катод.
Какво определя преминаването на електрически ток в течен проводник? Оказва се, че в такива разтвори (електролити) киселинните молекули (алкали, сол) под действието на разтворител (в този случай вода) се разпадат на две компоненти и една частица от молекулата има положителен електрически заряд, а другата отрицателен.
Частици от молекула, които имат електрически заряд, се наричат йони… Когато киселина, сол или алкал се разтварят във вода, в разтвора възникват голям брой както положителни, така и отрицателни йони.
Сега трябва да стане ясно защо през разтвора е преминал електрически ток, защото между електродите, свързани към източника на ток, a потенциална разликас други думи, един от тях се оказа положително таксуван, а другият отрицателен. Под влиянието на тази потенциална разлика положителните йони започнаха да се смесват към отрицателния електрод — катода, а отрицателните йони — към анода.
Така хаотичното движение на йони се е превърнало в подредено противоположно движение на отрицателни йони в едната посока и положителни йони в другата. Този процес на прехвърляне на заряд е поток от електрически ток през електролита и протича, докато има разлика в потенциала при електродите. С изчезването на потенциалната разлика, токът през електролита спира, подреденото движение на йони се нарушава и хаотичното движение започва отново.
Като пример, помислете за явлението електролиза, когато електрически ток преминава през разтвор на меден сулфат CuSO4 с медни електроди, спуснати в него.
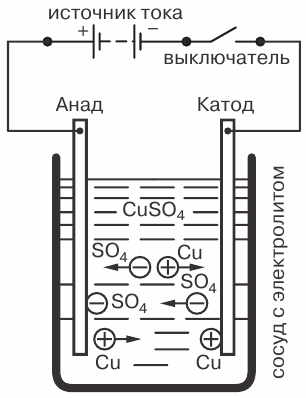
Явлението електролиза, когато токът преминава през разтвор на меден сулфат: С — съд с електролит, В — източник на ток, С — превключвател
Ще има и обратно движение на йони към електродите. Положителният йон ще бъде меден йон (Cu), а отрицателният йон ще бъде киселинният остатък (SO4). Медните йони, когато са в контакт с катода, ще бъдат разтоварени (прикрепяйки липсващите електрони към себе си), тоест те ще бъдат превърнати в неутрални молекули от чиста мед и ще бъдат отложени върху катода под формата на най -тънките ( молекулярен) слой.
Отрицателните йони, достигащи до анода, също се изхвърлят (даряват излишните електрони). Но в същото време те влизат в химическа реакция с медта на анода, в резултат на което към киселинния остатък SO4 се добавя медна молекула Сти и се образува молекула меден сулфат СнасО4се върна обратно към електролита.
Тъй като този химичен процес отнема много време, медта се отлага върху катода, който се освобождава от електролита. В този случай електролитът вместо медните молекули, които са отишли към катода, получава нови медни молекули поради разтварянето на втория електрод — анода.
Същият процес протича, ако вместо медни се вземат цинкови електроди, а електролитът е разтвор на цинков сулфат ZнSO4. Цинкът също ще бъде прехвърлен от анода към катода.
Поради това, разлика между електрически ток в метали и течни проводници се крие във факта, че в металите носителите на заряд са само свободни електрони, т.е. отрицателни заряди, докато в електролитите електричество пренасяни от противоположно заредени частици материя — йони, движещи се в противоположни посоки. Затова казват, че електролитите имат йонна проводимост.

Явлението електролиза е открит през 1837 г. от Б. С. Якоби, който прави множество експерименти за изследване и подобряване на химичните източници на ток. Якоби установява, че един от електродите, поставени в разтвор на меден сулфат, когато през него преминава електрически ток, е покрит с мед.
Това явление се нарича електроформоване, намира сега изключително голямо практическо приложение. Един пример за това е покритието на метални предмети с тънък слой от други метали, например никелиране, позлата, сребро и др.
Електрически ток в газове
Газовете (включително въздухът) не провеждат електричество при нормални условия. Например гол проводници за въздушни линиикато са окачени успоредно един на друг, те са изолирани един от друг чрез слой въздух.
Въпреки това, под въздействието на висока температура, голяма потенциална разлика и други причини, газовете, като течни проводници, йонизирайте, тоест в тях се появяват частици газови молекули в голям брой, които като носители на електричество допринасят за преминаването на електрически ток през газа.
Но в същото време йонизацията на газ се различава от йонизацията на течен проводник. Ако молекулата се разпадне на две заредени части в течност, тогава в газовете под действието на йонизацията електроните винаги се отделят от всяка молекула и йонът остава под формата на положително заредена част от молекулата.
Човек трябва само да спре йонизацията на газа, тъй като той престава да бъде проводим, докато течността винаги остава проводник на електрически ток. Следователно проводимостта на газ е временно явление, в зависимост от действието на външни причини.

Има обаче и друго вид електрически разрядНаречен дъгов разряд или просто електрическа дъга. Явлението електрическа дъга е открито в началото на 19 век от първия руски електроинженер В. В. Петров.
В.В.Правейки многобройни експерименти, Петров открива, че между два въглища, свързани към източник на ток, във въздуха се появява непрекъснат електрически разряд, придружен от ярка светлина. В своите писания В. В. Петров пише, че в този случай „тъмното спокойствие може да бъде достатъчно ярко осветено“. Така за първи път се получава електрическа светлина, която на практика се прилага от друг руски електроинженер Павел Николаевич Яблочков.
«Свещ Яблочков», чиято работа се основава на използването на електрическа дъга, направи по това време истинска революция в електротехниката.

Дъгов разряд днес се използва като източник на светлина, например в прожектори и проекционни устройства. Високата температура на дъговия разряд позволява да се използва за устройства за дъгови пещи… Понастоящем дъговите пещи, задвижвани от много голям ток, се използват в редица индустрии: за топене на стомана, чугун, феросплави, бронз и др. А през 1882 г. NN Benardos за първи път използва дъговия разряд за рязане и заваряване на метал.
В газовите тръби, флуоресцентни лампи, стабилизатори на напрежението, за получаване на електронни и йонни лъчи, т.нар разряд на светещ газ.
Искрен разряд Използва се за измерване на големи потенциални разлики с помощта на сферична искрова междина, чиито електроди са две метални топки с полирана повърхност. Топките се раздалечават и към тях се прилага измерима потенциална разлика. След това топките се сближават, докато между тях не премине искра. Познавайки диаметъра на топките, разстоянието между тях, налягането, температурата и влажността на въздуха, те откриват потенциалната разлика между топките според специални таблици. С този метод е възможно да се измери с точност от няколко процента от потенциалната разлика от порядъка на десетки хиляди волта.
