Принципът на измерване на рН, устройство и видове рН метри
За бързо определяне на нивото на рН (с други думи, нивото на киселинност) на различни среди се използват рН метри. Промишлена или питейна вода, разтвор на киселина, сол или алкали, кръв, урина и други телесни течности, плодове, зеленчуци и други хранителни продукти, медицински лекарства и т.н. — по принцип всичко може да стане обект на оперативно изследване рН стойност.
Измерването на PH е по същество измерване на активността на водородните йони в среда. И дори самото обозначение рН буквално се превежда от латинското „pondus Hydrogenii“ като „тегло на водорода“.
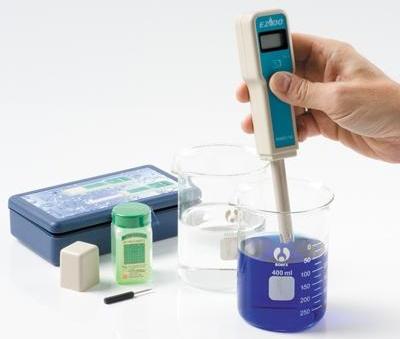
Днес рН метрите се използват широко в микробиологията и медицината, в пречистването на води и агрохимията, в почвознанието, в хидропониката, в лабораторните и полеви изследвания, в химическата и хранителната промишленост, в акваристиката и на много други места.
Съвременният рН метър ви позволява точно и бързо да определите стойността на рН. Ако рН е 7, средата е неутрална, като дестилирана вода, в която положителните водородни йони Н + и отрицателните хидроксидни йони ОН- са разделени по равно. Ако киселинността е повече от 7, тогава средата е алкална. Ако рН е по -малко от 7, средата е кисела.
И въпреки че химиците винаги са били в състояние да определят киселинността на средата по класическия метод, използвайки индикатори, например фенолфталеин, въпреки това в някои процеси е просто необходимо точно да се определи количествено този показател, а понякога е необходимо постоянно да се следи, за да се подреди да го коригирам. За това са измислени рН метри.
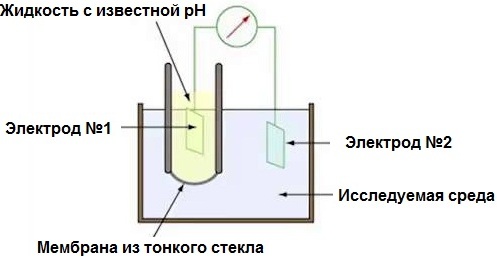
РН метърът всъщност е електронен миливолтметър, тъй като измерва потенциалната разлика в електрохимичната система от чифт електроди и изследваната среда, в която те са поставени. Вярно е, че скалата на устройството е градуирана тук не в миливолта, а в рН, тъй като измерената ЕМП се оказва пропорционална на рН.
Два електрода: стъклен индикатор (окислителите не се страхуват от боросиликатно стъкло) и сребърен хлорид — допълнителен референтен електрод. Стъкленият електрод има много високо съпротивление от десетки мегома и това е само основното изискване — съпротивлението на сондата да е не по -малко от 0,1 GΩ. РН метърът се калибрира с помощта на буферни разтвори с известно рН.
Поради факта, че стойността на ЕМП се влияе от температурата, всяко такова измервателно устройство има температурна компенсация за измервания при температури, различни от + 25 ° C. Но за да се постигне много висока точност, е необходимо да се измерва точно при температура от + 25 ° C, поради което много рН метри са оборудвани с вграден термометър, така че можете веднага да проследите температурата на средата в процес на проучване.
Индикаторният стъклен електрод под формата на тръба с тънкостенна топка в края, изработен от специално електропроводимо боросиликатно стъкло, по същество е свързан към електрическа верига. Движението на положителни Н + йони вътре в такова стъкло прави възможно използването му (катиони вътре в стъклото се движат спрямо полианиона на силициевата киселина). В епруветката се излива суспензия от сребърен хлорид в разтвор на солна киселина, след което там се потапя сребърна жица — така се получава електрод от сребърен хлорид.
Стъкленият електрод се спуска в изпитваната среда, електрическата верига се затваря чрез поставяне на допълнителен референтен електрод (живачно-каломелова паста в разтвор на калиев хлорид) в нея (чрез електролитен превключвател или директно). Калиевият хлорид създава контакт между живачно-каломеловата част на елемента и изпитваната среда. Този допълнителен електрод обикновено се поставя в стъклен корпус, който е непропусклив за Н + йони.
Проводящият контакт на разтвора на калиев хлорид в референтния електрод с изпитвания разтвор се образува поради тънка нишка или капиляра в стъклен корпус.По този начин се получава галванична клетка от референтен електрод и електрод от сребърен хлорид, а електролитната част на клетката включва проводим стъклен филм и среда за изпитване.
ЕМП на електродната система се измерва с миливолтметър, скалата му се градуира в рН. Електроните от електрода от сребърен хлорид се прехвърлят към референтния електрод под действието на измерената ЕМП, което винаги е придружено от прехвърляне на равен брой протони от вътрешната страна на стъкления електрод в средата.
Ако в този случай вземем концентрацията на положителни водородни йони Н + в константата на стъкления електрод, тогава ЕМП ще бъде функция от активността на Н +, тоест функция от рН на изследваната среда.
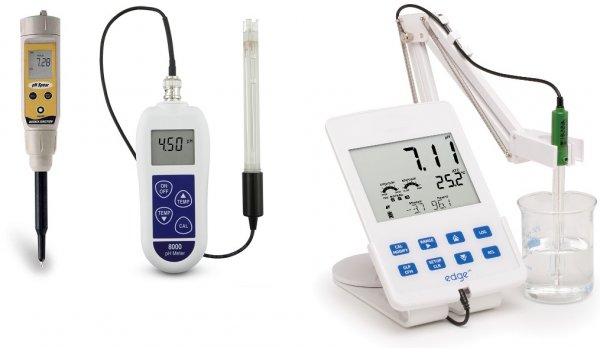
Съвременните модели на рН метри работят благодарение на микропроцесорите, които изпълняват температурната компенсация и решават много свързани задачи. Колкото по -сложно е устройството, толкова повече задачи може да реши. Класът на точност на инструментите варира в зависимост от модела и подходящ рН метър може да бъде избран за различни приложения.
Има джобни домакински рН -метри, има професионални лабораторни, преносими и промишлени стационарни. Някои рН-метри измерват концентрацията на йони в средата, съдържанието на нитрати и т.н., имат вградена памет за съхраняване на резултатите, възможност за комуникация с компютър и функция за коригиране на параметри чрез контур за обратна връзка.
